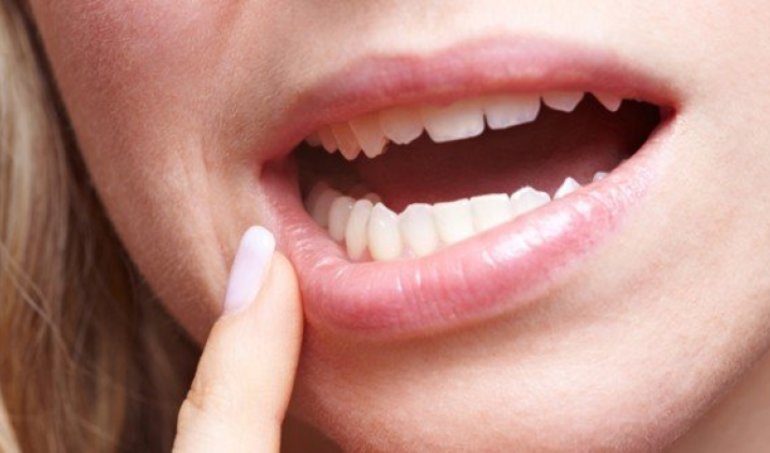
Se manifiesta como una inflamación al interior de la boca y la garganta con signos y síntomas como úlceras, dificultad y dolor al comer, producto de la toxicidad relacionada con la quimioterapia y radioterapia.-
Santiago, agosto de 2018.-Para la mayoría de las personas los efectos secundarios de los tratamientos antineoplásicos se resumen en caída del pelo, náuseas y vómitos, diarrea e hinchazón. Pero sólo para quienes se han sometido a terapias contra el cáncer saben que la inflamación y úlceras al interior de la boca y la garganta, también conocida como Mucositis oral, es uno de los principales problemas asociados a la quimio y radioterapia.
Estudios señalan que el 44% de los pacientes con cáncer sometidos a tratamientos con drogas antineoplásicas, el 80% de quienes reciben altas dosis de quimioterapia para el trasplante de médula, y alrededor del 97% de quienes reciben terapia de radiación para el cáncer de cabeza y cuello padecen de esta dolencia, la que se traduce en ulceraciones que impiden la alimentación, el habla y causan mucho dolor.
Como consecuencia, la mucositis oral constituye un factor de riesgo para infecciones; incluso es determinante en la prolongación o término anticipado al tratamiento y, por ende, lleva a la progresión o avance de la enfermedad de base, así como a un incremento en los costos asociados para el paciente y el sistema de salud.
Al respecto, el jefe de la unidad de medicina Oncológica del Instituto nacional del Tórax, Dr. Francisco Javier Orlandi, señala que la mucositis tiene mayor prevalencia en terapias que se efectúan con platinos (cis- carbo u oxali), con antraciclinas como doxorubicina, con ciclofosfamida e ifosfamida y fluoruracilo. “Esta corta lista, cubre un gran porcentaje de los tratamientos de los cánceres más frecuentes en Chile. Más allá de la calidad de vida,la mucositis oral impacta el posible retraso de los ciclos subsecuentes, lo que puede disminuir la eficacia de la terapia”.
Agrega que “la mala salud oral previa, la higiene bucal deficiente, las neutropenias intercurrentes (disminución aguda o crónica de granulocitos de la sangre que puede predisponer al organismo a contraer infecciones), pueden intensificar este efecto. Hasta ahora, las indicaciones de colutorios de diversa índole y los anestésicos locales son las indicaciones más frecuentes, sin embargo su eficiencia es pobre”.
Por este motivo es que en Chile el laboratorio biomédico Ingalfarma, que cuenta con el apoyo de CORFO, desarrolló el producto Dentoxol, una solución acuosa -de venta directa- que previene el avance de esta patología y que actualmente se encuentra en proceso de registro por la agencia regulatoria norteamericana FDA (Food and DrugAdministration). En formato de enjuague bucal, el tratamiento proporciona alivio temporal de la sequedad bucal, ayudando en el manejo del dolor producido por las llagas y úlceras, reemplazando físicamente la humedad y lubricando la cavidad oral.
Al usarse de forma profiláctica, Dentoxol se anticipa ala proliferación de las células basales del epitelio, estimuladas en respuesta al daño ocasionado por las terapias citotóxicas, preparando así la mucosa de manera efectiva contra el daño.
“En Chile tenemos una tarea importante que hacer: muy pocos hablan de la mucositis oral, que es invalidante y afecta de manera muy grave la calidad de vida de un paciente que ya está viviendo un proceso complejo de salud. Por lo tanto, hay un desafío de educar, además de prevenir y dar respuesta de manera oportuna”, señaló Felipe Galván, Ingeniero Químico y gerente general de la compañía.
Sobre Ingalfarma
Ingalfarma es un laboratorio biomédico fundado en Chile en el año 2006 por el Ingeniero Químico Felipe Galván, junto a su padre, el Dr. Tomás Galván, cuyo objetivo es desarrollar soluciones a patologías orales de difícil pronóstico o tratamiento. Su misión es desarrollar y comercializar productos biomédicos innovadores que reivindiquen el valor de la salud oral, un segmento poco explorado por la industria biomédica.
Con el apoyo de CORFO, Ingalfarma creó el producto Dentoxol, que ya se comercializa en nuestro país y se abre puertas en el mundo, y el que actualmente se encuentra en trámite de aprobación por la FDA, en Estados Unidos y EMA en la Unión Europea.
Mucositis oral, laboratorio chileno da importante avance en la solución del problema asociado al cáncer